Công thức Lewis của CH4
Bài viết hướng dẫn cách viết Công thức Lewis của CH4 theo chương trình sách mới Kết nối tri thức, Cánh diều, Chân trời sáng tạo giúp học sinh dễ dàng nắm vững cách viết Công thức Lewis của CH4.
Công thức Lewis của CH4
Methane (CH4) là một hợp chất cộng hóa trị. Phân tử CH4 được tạo thành do sự góp chung các electron hóa trị. Vậy cách biểu diễn công thức electron, công thức Lewis và công thức cấu tạo của CH4 như thế nào. Các em hãy theo dõi bài viết sau.
1. Công thức electron của CH4
- Sự tạo thành phân tử CH4: Nguyên tử hydrogen (H) có cấu hình electron là 1s1, nguyên tử carbon (C) có cấu hình electron là 1s22s22p2. Để đạt được cấu hình electron bền vững của khí hiếm gần nhất, nguyên tử C cần thêm 4 electron, mỗi nguyên tử H cần thêm 1 electron. Khi hình thành phân tử CH4, mỗi nguyên tử H góp chung 1 electron với nguyên tử C, 4 nguyên tử H sẽ tạo thành 4 cặp electron dùng chung với nguyên tử C.
- Công thức electron của CH4 là:
- Nhận xét:
+ Phân tử CH4 có 4 cặp electron dùng chung. Cặp electron chung không bị lệch về phía nguyên tử nào.
+ Trong phân tử CH4 không có electron tự do.
2. Công thức Lewis của CH4
a) Cách 1: Viết công thức Lewis dựa vào công thức electron
Từ công thức electron, thay 1 cặp electron dùng chung bằng 1 gạch nối giữa hai nguyên tử ta được công thức Lewis
Từ công thức electron của CH4 ta thấy mỗi nguyên tử H liên kết với nguyên tử C bằng 1 cặp electron, ta thay mỗi cặp electron này bằng một gạch nối “–”. Ta được công thức Lewis của CH4 là:
b) Cách 2: Thực hiện lần lượt theo các bước sau
Bước 1: Tính tổng số electron hóa trị trong phân tử
Carbon (C) có 4 electron hóa trị, hydrogen có 1 electron hóa trị. Trong phân tử CH4 có 1 nguyên tử C và 4 nguyên tử H.
Vậy tổng số electron hóa trị = 4 + 4.1 = 8 electron
Bước 2: Vẽ khung phân tử tạo bởi liên kết đơn giữa các nguyên tử
Trong phân tử CH4, nguyên tử C cần 4 electron để đạt octet, mỗi nguyên tử H cần 1 electron để đạt octet. Vì vậy, C là nguyên tử trung tâm, còn các nguyên tử H được xếp xung quanh:
Bước 3: Tính số electron hóa trị chưa tham gia liên kết bằng cách lấy tổng số electron trừ số electron tham gia tạo liên kết.
Số electron hóa trị chưa tham gia liên kết trong sơ đồ là: 8 – 2.4 = 0
Từ công thức (1), nguyên tử H và C đều đã đủ octet.
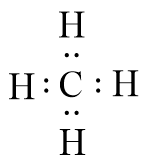
Vậy công thức Lewis của CH4 là:
- Nhận xét:
+ ∆χ(C – H) = |2,55 – 2,2| = 0,35 < 0,4 ⇒ Liên kết trong phân tử CH4 thuộc loại liên kết cộng hóa trị không phân cực.
+ Liên kết C – H được tạo thành do sự xen phủ orbital s – p.
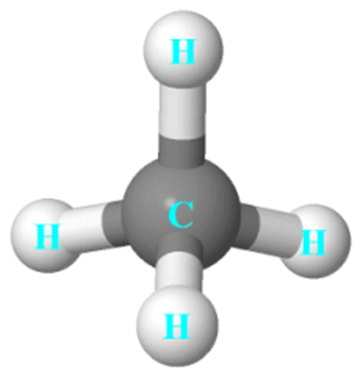
+ Phân tử CH4 có dạng tứ diện đều.
3. Cách viết công thức cấu tạo
Từ công thức Lewis, ta loại bỏ đi các electron tự do (electron không tham gia liên kết) thu được công thức cấu tạo.
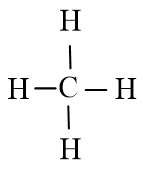
- Công thức cấu tạo của CH4 là:
- Nhận xét:
+ Trong phân tử CH4 có 4 liên kết đơn C – H.
+ Công thức Lewis của CH4 trùng với công thức cấu tạo do các nguyên tử đều không còn electron riêng.
4. Ví dụ minh họa
Câu 1. Liên kết nào dưới đây là liên kết cộng hóa trị không phân cực?
A. Na – O
B. O – H
C. Na – C
D. C – H
Hướng dẫn giải
Đáp án đúng là: D
Liên kết C – H có hiệu độ âm điện giữa hai nguyên tử tham gia liên kết là
|3,16 – 2,96| = 0,2 < 0,4 nên là liên kết cộng hóa trị không phân cực.
Câu 2. Trong phân tử methane (CH4) số cặp electron chung giữa nguyên tử carbon (C) và các nguyên tử hydrogen (H) là
A. 3
B. 2
C. 1
D. 4
Hướng dẫn giải
Đáp án đúng là: D
Nguyên tử hydrogen (H) có cấu hình electron là 1s1, nguyên tử carbon (C) có cấu hình electron là 1s22s22p2. Để đạt được cấu hình electron bền vững của khí hiếm gần nhất, nguyên tử C cần thêm 4 electron, mỗi nguyên tử H cần thêm 1 electron. Khi hình thành phân tử CH4, mỗi nguyên tử H góp chung 1 electron với nguyên tử C, 4 nguyên tử H sẽ tạo thành 4 cặp electron dùng chung với nguyên tử C.
Xem thêm cách viết công thức Lewis của một số chất hay, chi tiết khác:
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)

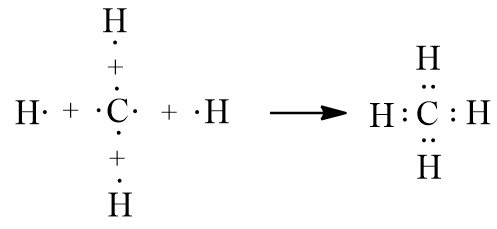







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



