Tìm hiểu tính chất hoá học của muối
Khoa học tự nhiên lớp 8 Bài 11: Muối
Hoạt động trang 50 Khoa học tự nhiên 8: Tìm hiểu tính chất hoá học của muối
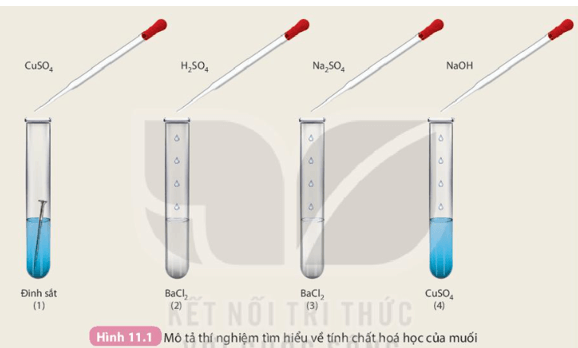
Chuẩn bị: Các dung dịch: H2SO4 loãng, NaOH loãng, Na2SO4, CuSO4; 4 ống nghiệm: ống (1) chứa 1 đinh sắt đã được làm sạch, ống (2) và (3) mỗi ống nghiệm chứa khoảng 1 mL dung dịch BaCl2, ống (4) chứa khoảng 1 mL dung dịch CuSO4.
Tiến hành: ống (1) cho khoảng 2 mL dung dịch CuSO4; ống (2) cho khoảng 1 mL dung dịch H2SO4; ống (3) cho khoảng 1 mL dung dịch Na2SO4; ống (4) cho khoảng 1 mL dung dịch NaOH
Quan sát hiện tượng xảy ra ở mỗi ống nghiệm và thực hiện yêu cầu:
1. Viết phương trình hoá học, giải thích hiện tượng xảy ra.
2. Thảo luận nhóm rút ra kết luận về tính chất hoá học của muối.
Trả lời:
1.
+ Ống nghiệm 1:
Hiện tượng: Đinh sắt tan dần, có lớp kim loại màu đỏ bám ngoài đinh sắt; Dung dịch trong ống nghiệm nhạt màu dần.
Phương trình hoá học: Fe + CuSO4 → FeSO4 + Cu.
+ Ống nghiệm 2:
Hiện tượng: Xuất hiện kết tủa trắng.
Phương trình hoá học: BaCl2 + H2SO4 → BaSO4 + 2HCl.
+ Ống nghiệm 3:
Hiện tượng: Xuất hiện kết tủa trắng.
Phương trình hoá học: BaCl2 + Na2SO4 → BaSO4 + 2NaCl.
+ Ống nghiệm 4:
Hiện tượng: Xuất hiện kết tủa xanh, dung dịch nhạt màu dần.
Phương trình hoá học: CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4.
2. Một số tính chất hoá học của muối:
- Dung dịch muối có thể tác dụng với một số kim loại tạo thành muối mới và kim loại mới. Ví dụ: Fe + CuSO4 → FeSO4 + Cu.
- Muối có thể tác dụng với một số dung dịch acid tạo thành muối mới và acid mới. Sản phẩm của phản ứng tạo thành có ít nhất một chất là chất khí/ chất ít tan/ không tan … Ví dụ: BaCl2 + H2SO4 → BaSO4 + 2HCl.
- Dung dịch muối tác dụng với dung dịch base tạo thành muối mới và base mới, trong đó có ít nhất một sản phẩm là chất khí/ chất ít tan/ không tan … Ví dụ:
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4.
- Hai dung dịch muối tác dụng với nhau tạo thành hai muối mới, trong đó có ít nhất một muối không tan hoặc ít tan. Ví dụ:
BaCl2 + Na2SO4 → BaSO4 + 2NaCl.
Lời giải KHTN 8 Bài 11: Muối hay khác:
- Mở đầu trang 48 Bài 11 Khoa học tự nhiên 8: Muối có rất nhiều ứng dụng trong đời sống như làm phân bón, bảo quản thực phẩm, làm bột nở cho các loại bánh, gia vị,… Muối có những tính chất hoá học nào và được điều chế như thế nào?....
- Hoạt động trang 48 Khoa học tự nhiên 8: Tìm hiểu về các phản ứng tạo muối....
- Câu hỏi 1 trang 49 Khoa học tự nhiên 8: Viết công thức của các muối sau: potassium sulfate, sodium hydrogensulfate, sodium hydrogencarbonate, sodium chloride, sodium nitrate, calcium hydrogenphosphate, magnesium sulfate, copper(II) sulfate.....
- Câu hỏi 2 trang 49 Khoa học tự nhiên 8: Gọi tên các muối sau: AlCl3; KCl; Al2(SO4)3; MgSO4; NH4NO3; NaHCO3.....
- Câu hỏi 3 trang 49 Khoa học tự nhiên 8: Viết phương trình hoá học của phản ứng tạo thành muối KCl và MgSO4.....
- Câu hỏi trang 51 Khoa học tự nhiên 8: Trong dung dịch, giữa các cặp chất nào sau đây có xảy ra phản ứng? Viết phương trình hoá học của các phản ứng đó....
- Câu hỏi trang 52 Khoa học tự nhiên 8: Tính chất hoá học của các hợp chất vô cơ được tóm tắt bằng sơ đồ dưới đây:....
Các bài học để học tốt KHTN 8 Bài 11: Muối:
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 8 Kết nối tri thức hay, chi tiết khác:
Xem thêm các tài liệu học tốt lớp 8 hay khác:
- Giải sgk Khoa học tự nhiên 8 Kết nối tri thức
- Giải SBT KHTN 8 Kết nối tri thức
- Giải lớp 8 Kết nối tri thức (các môn học)
- Giải lớp 8 Chân trời sáng tạo (các môn học)
- Giải lớp 8 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Giải KHTN lớp 8 Kết nối tri thức của chúng tôi được biên soạn bám sát nội dung và hình ảnh sách giáo khoa Khoa học tự nhiên 8 Kết nối tri thức với cuộc sống (NXB Giáo dục).
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 8 (hay nhất) - KNTT
- Soạn văn 8 (ngắn nhất) - KNTT
- Giải sgk Toán 8 - KNTT
- Giải Tiếng Anh 8 Global Success
- Giải sgk Tiếng Anh 8 Smart World
- Giải sgk Tiếng Anh 8 Friends plus
- Giải sgk Khoa học tự nhiên 8 - KNTT
- Giải sgk Lịch Sử 8 - KNTT
- Giải sgk Địa Lí 8 - KNTT
- Giải sgk Giáo dục công dân 8 - KNTT
- Giải sgk Tin học 8 - KNTT
- Giải sgk Công nghệ 8 - KNTT
- Giải sgk Hoạt động trải nghiệm 8 - KNTT
- Giải sgk Âm nhạc 8 - KNTT






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

