Cấu hình electron của O, oxygen (oxi) chương trình mới
Bài viết hướng dẫn cách viết Cấu hình electron của O, oxygen (oxi) theo chương trình sách mới của ba bộ sách Kết nối tri thức, Cánh diều, Chân trời sáng tạo giúp học sinh dễ dàng nắm vững cách viết Cấu hình electron của O, oxygen (oxi).
Cấu hình electron của O, oxygen (oxi) chương trình mới
Oxygen (oxi) là nguyên tố rất quan trọng trong cuộc sống của chúng ta. Oxygen cũng thường xuyên xuất hiện trong các bài tập hóa học. Bài viết dưới đây sẽ giúp các em viết được cấu hình electron nguyên tử oxygen, cấu hình electron nguyên tử oxygen theo ô orbital, từ đó tìm ra mối liên hệ giữa cấu hình electron với vị trí trong bảng tuần hoàn và một số tính chất của nguyên tố này.
1. Cấu hình electron nguyên tử oxygen (Z = 8)
- Nguyên tố oxygen có kí hiệu hóa học là O.
- Nguyên tử oxygen có số hiệu nguyên tử là 8 ⇒ nguyên tử oxygen có 8 electron.
- Cấu hình electron nguyên tử oxygen là 1s22s22p4.
Viết gọn: [He]2s22p4.
2. Cấu hình electron nguyên tử oxygen (Z = 8) theo ô orbital.
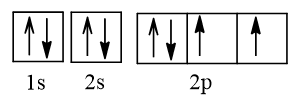
- Cấu hình electron nguyên oxygen (Z = 8) theo ô orbital là:
- Ở trạng thái cơ bản nguyên tử O có 2 electron độc thân, thuộc AO 2p.
3. Mối liên hệ giữa cấu hình electron với vị trí trong bảng tuần hoàn và tính chất nguyên tố
- Vị trí của oxygen trong bảng tuần hoàn:
Từ cấu hình electron của oxygen là 1s22s22p4 ta xác định được:
+ Oxygen thuộc ô thứ 8 (do Z = 8)
+ Chu kì 2 (do có 2 lớp electron)
+ Nhóm VIA (do có 6 electron hóa trị, nguyên tố p).
+ Là nguyên tố p (do có cấu hình electron lớp ngoài cùng là 2s22p4).
- Tính chất nguyên tố:
+ Oxygen là phi kim hoạt động mạnh.
+ Oxygen có xu hướng nhận 2 electron khi tham gia phản ứng hóa học để đạt cấu hình bền vững của Ne.
O + 2e ⟶ O2-
4. Ví dụ
Câu 2: Nguyên tử X có cấu hình electron phân lớp ngoài cùng là 2p4. Xác định vị trí của X trong bảng tuần hoàn?
A. Nằm ở ô thứ 6, chu kì 2, nhóm IVA.
B. Nằm ở ô thứ 7, chu kì 2, nhóm VA.
C. Nằm ở ô thứ 8, chu kì 2, nhóm VIA.
D. Nằm ở ô thứ 9, chu kì 2, nhóm VIIA.
Lời giải:
Đáp án đúng là: C
Nguyên tử X có cấu hình electron phân lớp ngoài cùng là 2p4.
⇒ Cấu hình electron đầy đủ của nguyên tử X là 1s22s22p4.
⇒ Nguyên tố X thuộc ô thứ 8 (Z = 8), chu kì 2 (có 2 lớp electron), nhóm VIA (6 electron hóa trị).
Câu 2. Nguyên tử của nguyên tố M có cấu hình electron là 1s22s22p4. Số electron độc thân của M ở trạng thái cơ bản là
A. 3
B. 2
C. 1
D. 0
Lời giải:
Đáp án đúng là: B
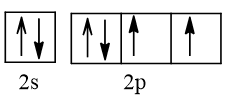
Cấu hình electron lớp ngoài cùng biểu diễn trên AO là:
⇒ Có 2 electron độc thân ở trạng thái cơ bản.
Xem thêm cách viết cấu hình electron của các ion hay, chi tiết khác:
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



