So sánh bán kính của Na và Na+
Bán kính nguyên tử natri và bán kính ion Na+ bán kính nào lớn hơn? Bài viết sau sẽ giúp các em giải quyết vấn đề này.
So sánh bán kính của Na và Na+
1. So sánh
Bán kính nguyên tử natri lớn hơn bán kính ion Na+.
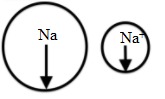
2. Giải thích
Ta có, cấu hình electron của ion Na+ là 1s2 2s2 2p6.
⇒ Nguyên tử Na đã nhường 1 electron lớp ngoài cùng để hình thành ion Na+.
⇒ Bán kính của ion Na+ nhỏ hơn bán kính của nguyên tử Na.
Giải thích: Cả nguyên tử Na và ion Na+ đều có điện tích hạt nhân là 11+. Mà nguyên tử Na có 11 electron còn ion Na+ có 10 electron nên hạt nhân của ion Na+ sẽ hút các electron mạnh hơn làm cho bán kính ion nhỏ hơn.
3. Ví dụ minh họa
Nhận xét nào sau đây là đúng?
A. Bán kính nguyên tử Na lớn hơn bán kính ion Na+.
B. Bán kính ion K+ lớn hơn bán kính nguyên tử K.
C. Ion Na+ có 18 electron.
D. Bán kính của nguyên tử Al và ion Al3+ là bằng nhau.
Hướng dẫn giải
Đáp án đúng là: A
B sai, bán kính ion K+ nhỏ hơn bán kính nguyên tử K.
C sai, ion Na+ có 10 electron.
D sai, bán kính ion Al3+ nhỏ hơn bán kính nguyên tử Al
Xem thêm các bài viết về cách so sánh bán kính nguyên tử và ion hay, chi tiết khác:
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



