3+ Đề thi Học kì 1 Hoá học 11 Chân trời sáng tạo (cấu trúc mới, có đáp án)
Với bộ 3+ Đề thii Hoá học 11 Học kì 1 Chân trời sáng tạo năm 2026 theo cấu trúc mới có đáp án và ma trận được biên soạn và chọn lọc từ đề thi Hoá học 11 của các trường THPT trên cả nước sẽ giúp học sinh lớp 11 ôn tập và đạt kết quả cao trong các bài thi Học kì 1 Hoá học 11.
3+ Đề thi Học kì 1 Hoá học 11 Chân trời sáng tạo (cấu trúc mới, có đáp án)
Chỉ từ 150k mua trọn bộ Đề thi Học kì 1 Hoá học 11 Chân trời sáng tạo theo cấu trúc mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
Sở Giáo dục và Đào tạo ...
Đề thi Học kì 1 - Chân trời sáng tạo
Năm học ...
Môn: Hoá học lớp 11
Thời gian làm bài: phút
(Đề số 1)
A. Phần trắc nghiệm (7 điểm)
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 12. Mỗi câu hỏi thí sinh chỉ chọn một phương án. (3 điểm)
Câu 1. Trong tự nhiên, nguyên tố nitrogen có hai đồng vị bền là và (0,37%). Nguyên tử khối trung bình của nitrogen gần nhất với
A. 14,000.
B. 14,004.
C. 14,037.
D. 14,063.
Câu 2. Phân biệt được đung dịch NH4Cl và NaCl bằng thuốc thử là dung dịch
A. KCl.
B. KNO3.
C. KOH.
D. K2SO4.
Câu 3. Cho Iron(III) oxide tác dụng với nitric acid thì sản phẩm thu được là
A. Fe(NO3)3, NO và H2O.
B. Fe(NO3)3, NO2 và H2O.
C. Fe(NO3)3, N2 và H2O.
D. Fe(NO3)3 và H2O.
Câu 4. Cho phản ứng: SO2 + Cl2 + 2H2O H2SO4 + 2HCl. Trong phản ứng SO2 đóng vai trò là
A. chất oxi hoá.
B. chất khử.
C. môi trường.
D. vừa là chất khử vừa là chất oxi hoá.
Câu 5. Sulfur trioxide được điều chế theo phương trình hóa học:
Cho các biện pháp (1) tăng nhiệt độ, (2) tăng áp suất chung của hệ phản ứng, (3) hạ nhiệt độ, (4) dùng thêm chất xúc tác V2O5, (5) giảm nồng độ SO3, (6) giảm áp suất chung của hệ phản ứng. Những biện pháp nào làm cân bằng trên chuyển dịch theo chiều thuận?
A. (1), (2), (4), (5).
B. (2), (3), (5).
C. (2), (3), (4), (6).
D. (1), (2), (4).
Câu 6. Theo thuyết Bronsted - Lowry, H2O đóng vai trò gì trong phản ứng sau:
A. Chất oxi hóa.
B. Chất khử.
C. Acid.
D. Base.
Câu 7. Dãy chất nào sau đây là hợp chất hữu cơ?
A. (NH4)2CO3, CO2, CH4, C2H6.
B. C2H4, CH4, C2H6O, C3H9N.
C. CO2, K2CO3, NaHCO3, C2H5Cl.
D. NH4HCO3, CH3OH, CH4, CCl4.
Câu 8. Phương pháp nào sau đây không phải là phương pháp tách biệt và tinh chế hợp chất hữu cơ?
A. Phương pháp điện phân.
B. Phương pháp chiết
C. Phương pháp kết tinh.
D. Sắc kí cột.
Câu 9. Chất nào sau đây có công thức phân tử trùng với công thức đơn giản nhất?
A. CH3COOH.
B. C6H6.
C. C2H4Cl2.
D. C2H5OH.
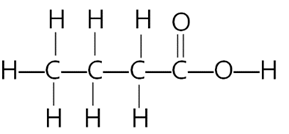
Câu 10. Cho công thức cấu tạo sau:
Công thức cấu tạo thu gọn của hợp chất là
A. CH3CH2CH2COOH.
B. CH3CH2COOH.
C. CH3CH2CH2OH.
D. CH3CH2CHOHCHO.
Câu 11. Phân tích thành phần hợp chất X thu được phần trăm khối lượng các nguyên tố như sau: %C = 34,62; %H = 3,84; còn lại là oxygen. Từ phổ MS người ta xác định được phân tử khối của X là 104. Công thức phân tử của X là
A. CHO.
B. C3H4O4.
C. C4H3O3.
D. C3H4O2.
Câu 12. Khí nitrogen và khí oxygen là hai thành phần chính của không khí. Trong kĩ thuật người ta có thể hạ thấp nhiệt độ để hóa lỏng không khí. Biết nitrogen lỏng sôi ở -196oC oxygen lỏng sôi ở -183oC. Phương pháp tách riêng khí nitrogen và oxygen là
A. lọc.
B. chiết.
C. cô cạn.
D. chưng cất.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 2. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (2 điểm)
Câu 1. Tiến hành thí nghiệm sau:
Bước 1: Cho khoảng 2 gam phân bón ammonium chloride vào ống nghiệm. Sau đó cho khoảng 2 mL nước cất vào ống nghiệm, lắc đều đến khi tan hết.
Bước 2: Cho khoảng 2 mL dung dịch NaOH đặc vào ống nghiệm, lắc đều rồi đun nóng nhẹ trên ngọn lửa đèn cồn.
Bước 3: Đặt mẫu giấy quỳ tím đã tẩm ướt lên miệng ống nghiệm đang đun.
a. Thí nghiệm trên chứng minh muối ammonium chloride dễ tan trong nước ở nhiệt độ thường.
b. Có thể sử dụng dung dịch kiềm để nhận biết ion .
c. Mẫu giấy quỳ tím chuyển sang màu đỏ.
d. Nếu thay ammonium chloride bằng ammonium sulfate, thì hiện tượng ở bước 3 vẫn tương tự.
Câu 2. Cho các phát biểu sau:
a. Công thức CH3 – CH2 = OH phù hợp với thuyết cấu tạo hóa học.
b. Theo thuyết cấu tạo hóa học C trong hợp chất hữu cơ có thể có hóa trị IV hoặc II.
c. Công thức CH3 – CH2 – CH2 – N không phù hợp với thuyết cấu tạo hóa học.
d. CH3CH2Cl là dẫn xuất của hydrocarbon.
PHẦN III. Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 4. (2 điểm)
Câu 1. Cho phương trình nhiệt hóa học:
3H2(g) + N2(g) NH3(g) = -91,80kJ
Lượng nhiệt tỏa ra khi dùng 9 g H2 (g) để tạo thành NH3 (g) là bao nhiêu kJ?
Câu 2. Trong công nghiệp thực phẩm, nitrogen lỏng (D = 0,808 g/mL) được phun vào vỏ bao bì trước khi đóng nắp để làm căng vỏ bao bì. Thể tích khí nitrogen thu được (đkc) khi hóa hơi 1 mL nitrogen lỏng là bao nhiêu mL? (Kết quả làm tròn đến hàng phần mười)
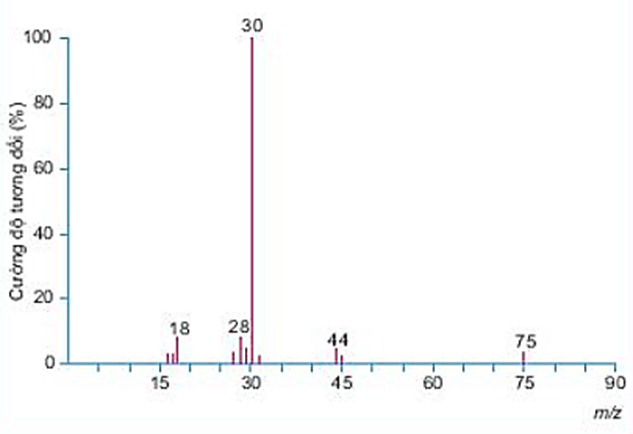
Câu 3. Một hợp chất hữu cơ Y có 32% C; 6,67% H; 18,67% N về khối lượng còn lại là O. Phân tử khối của hợp chất này được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất. Biết phổ khối lượng của Y được cho ở hình bên dưới:
Số lượng các nguyên tử có trong 1 phân tử Y là?
Câu 4. Số đồng phân cấu tạo có thể có của hợp chất có công thức phân tử là C4H10O?
B. Phần tự luận (3 điểm)
Câu 1. Cho phương trình hóa học sau:
Biết rằng, ở 760 °C các chất đều ở thể khí và nồng độ mol của CH4, H2O, H2 và CO ở trạng thái cân bằng lần lượt là 0,126M; 0,242M; 1,150M và 0,126M.
Tính hằng số cân bằng Kc của phản ứng ở 760 °C. (Làm tròn đến hàng phần trăm)
Câu 2. Nêu cách pha loãng H2SO4 đặc an toàn trong phòng thí nghiệm?
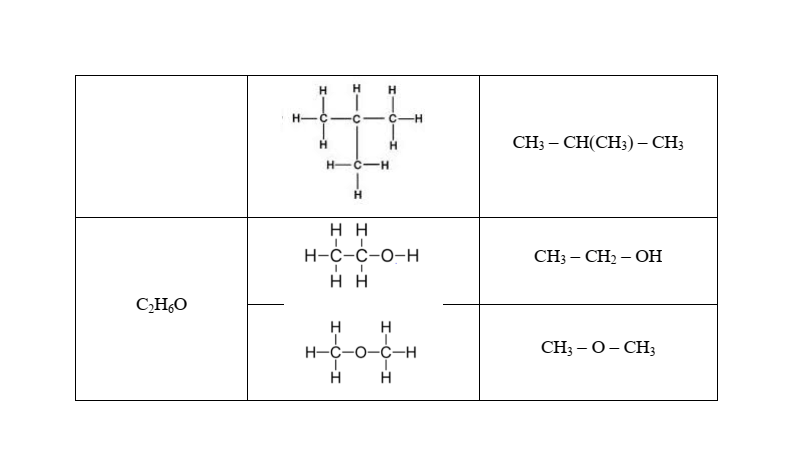
Câu 3. Viết công thức cấu tạo (đầy đủ và thu gọn) của các chất có công thức phân tử như sau: C4H10, C2H6O.
Sở Giáo dục và Đào tạo ...
Đề thi Học kì 1 - Chân trời sáng tạo
Năm học ...
Môn: Hoá học lớp 11
Thời gian làm bài: phút
(Đề số 2)
I. PHẦN TRẮC NGHIỆM (7,0 điểm)
Câu 1. Phản ứng thuận nghịch là phản ứng
A. xảy ra theo hai chiều ngược nhau trong cùng điều kiện.
B. có phương trình hoá học được biểu diễn bằng mũi tên một chiều.
C. chỉ xảy ra theo một chiều nhất định.
D. xảy ra giữa hai chất khí.
Câu 2. Cho các nhận xét sau:
(a) Ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản nghịch.
(b) Ở trạng thái cân bằng, các chất không phản ứng với nhau.
(c) Ở trạng thái cân bằng, nồng độ chất sản phẩm luôn lớn hơn nồng độ chất ban đầu.
(d) Ở trạng thái cân bằng, nồng độ các chất không thay đổi.
Các nhận xét đúng là
A. (a) và (b).
B. (b) và (c).
C. (a) và (c).
D. (a) và (d).
Câu 3. Chất nào dưới đây không phân li ra ion khi hòa tan trong nước?
A. MgCl2.
B. HClO3.
C. Ba(OH)2.
D. C6H12O6 (glucose).
Câu 4. Môi trường base là môi trường có
A. [H+] < [OH−].
B. [H+] > [OH−].
C. [H+] = [OH−].
D. [H+] > 1,0.10−7.
Câu 5. Ở nhiệt độ thường, nitrogen khá trơ về mặt hoạt động hóa học là do
A. nitrogen có bán kính nguyên tử nhỏ.
B. nitrogen có độ âm điện lớn.
C. phân tử nitrogen có liên kết ba bền vững.
D. phân tử nitrogen không phân cực.
Câu 6. Trong các phát biểu sau, phát biểu nào không đúng?
A. NH3 là chất khí không màu, không mùi, tan ít trong nước.
B. Khí NH3 nặng hơn không khí.
C. Khí NH3 dễ hoá lỏng, tan nhiều trong nước.
D. Phân tử NH3 chứa các liên kết cộng hoá trị phân cực.
Câu 7. Thành phần chính của quặng galena là
A. PbS.
B. FeS2.
C. CaSO4.
D. BaSO4.
Câu 8. Sulfur được dân gian sử dụng để pha chế vào thuốc trị các bệnh ngoài da. Tên gọi dân gian của sulfur là
A. diêm sinh.
B. đá vôi.
C. phèn chua.
D. giấm ăn.
Câu 9. Bước sơ cứu đầu tiên cần làm ngay khi bị bỏng acid là
A. rửa ngay bằng nước sạch khoảng 20 phút.
B. trung hoà acid bằng kiềm đặc.
C. băng bó tạm thời vết bỏng.
D. đưa đến cơ sở y tế gần nhất.
Câu 10. Chất nào sau đây được dùng làm chất phụ gia để làm đông các sản phẩm như đậu hũ, đậu non…?
A. BaSO4.
B. CaSO4.
C. MgSO4.
D. (NH4)2SO4.
Câu 11. Nhận xét nào dưới đây về đặc điểm chung của các chất hữu cơ không đúng?
A. Các hợp chất hữu cơ thường khó bay hơi, bền với nhiệt và khó cháy.
B. Liên kết hoá học chủ yếu trong các phân tử hợp chất hữu cơ là liên kết cộng hoá trị.
C. Các hợp chất hữu cơ thường không tan hoặc ít tan trong nước, tan trong dung môi hữu cơ.
D. Các phản ứng hoá học của hợp chất hũu cơ thường xảy ra chậm và theo nhiều hướng khác nhau tạo ra một hỗn hợp các sản phẩm.
Câu 12. Hợp chất hữu cơ là các hợp chất của....... (trừ các oxide của carbon, muối carbonate, cyanide, carbide,...). Từ thích hợp điền vào chỗ trống trong định nghĩa trên là
A. carbon.
B. hydrogen.
C. oxygen.
D. nitrogen.
Câu 13. Phương pháp chiết là sự tách chất dựa vào sự khác nhau
A. về kích thước phân tử.
B. ở mức độ nặng nhẹ về khối lượng.
C. về khả năng bay hơi.
D. về khả năng tan trong các dung môi khác nhau.
Câu 14. Phương pháp kết tinh được ứng dụng trong trường hợp nào dưới đây?
A. Làm đường cát, đường phèn từ mía.
B. Giã cây chàm, cho vào nước, lọc lấy dung dịch màu để nhuộm sợi, vải.
C. Nấu rượu để uống.
D. Ngâm rượu thuốc.
Câu 15. Hydrocarbon là loại hợp chất hữu cơ mà thành phần phân tử có các nguyên tố nào sau đây?
A. C và H.
B. C, H và O.
C. C, H và N.
D. C, H, O và N.
Câu 16. Các chất hữu cơ có tính chất hoá học tương tự nhau và thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 được gọi là các chất
A. đồng phân của nhau.
B. đồng đẳng của nhau.
C. đồng vị của nhau.
D. đồng khối của nhau.
Câu 17. Cho phản ứng sau: 2C(s) + O2(g) ⇌ 2CO(g). Biểu thức hằng số cân bằng KC của phản ứng là
A. KC =
B. KC =
C. KC =
D. KC =
Câu 18. Cho phương trình: CH3COOH + H2O ⇌ CH3COO− + H3O+
Trong phản ứng nghịch, theo thuyết Bronsted – Lowry chất nào là acid?
A. CH3COOH.
B. H2O.
C. CH3COO−.
D. H3O+.
Câu 19. Phân biệt được đung dịch NH4Cl và NaCl bằng thuốc thử là dung dịch
A. KCl.
B. KNO3.
C. KOH.
D. K2SO4.
Câu 20. Trong những cơn mưa dông kèm sấm sét, nitrogen kết hợp trực tiếp với oxygen tạo thành sản phẩm là
A. NO.
B. N2O.
C. NH3.
D. NO2.
Câu 21. Số oxi hoá của N trong HNO3 là
A. +1.
B. +3.
C. +5.
D. +7.
Câu 22. Chất khí (X) tan trong nước tạo ra dung dịch làm quỳ tím hoá đỏ và khí (X) có thể được dùng làm chất tẩy màu. Khí (X) là
A. NH3.
B. CO2.
C. SO2.
D. O3.
Câu 23. Cho kim loại sắt tác dụng với acid H2SO4 đặc, nóng. Khí sinh ra có tên gọi là
A. khí oxygen.
B. khí hydrogen.
C. khí carbonic.
D. khí sulfur dioxide.
Câu 24. Phổ hồng ngoại là phương pháp vật lí rất quan trọng và phổ biến để nghiên cứu về
A. thành phần nguyên tố chất hữu cơ.
B. thành phần phân tử hợp chất hữu cơ.
C. cấu tạo hợp chất hữu cơ.
D. cấu trúc không gian hợp chất hữu cơ.
Câu 25. Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36 °C), heptane (sôi ở 98 °C), octane (sôi ở 126 °C) và nonane (sôi ở 151 °C). Có thể tách riêng các chất đó bằng cách nào sau đây?
A. Chiết.
B. Kết tinh.
C. Bay hơi.
D. Chưng cất.
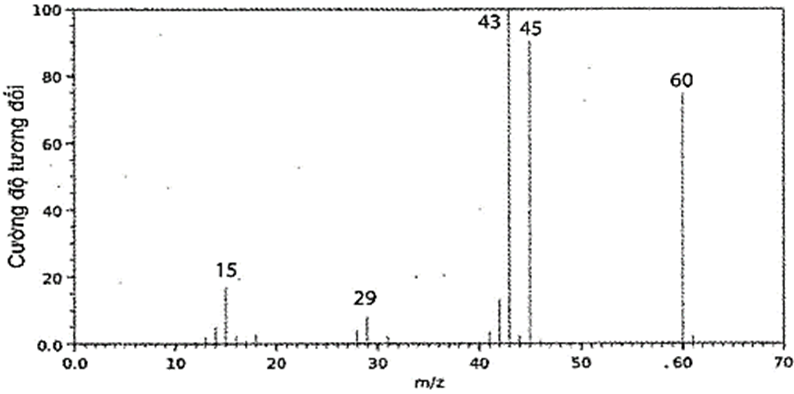
Câu 26. Phổ khối lượng của hợp chất hữu cơ X được cho như hình vẽ bên dưới:
Phân tử khối của hợp chất hữu cơ X là
A. 45.
B. 60.
C. 43.
D. 15.
Câu 27. Công thức hoá học nào sau đây không phù hợp với thuyết cấu tạo hoá học?
A. CH3 – CH2 – OH.
B. CH3–O=CH–CH3.
C. CH3 – CH2 – CH2 – NH2.
D. CH3Cl.
Câu 28. Cặp chất nào dưới đây là đồng phân loại nhóm chức?
A. CH3COCH3 và CH3CH2CH2OH.
B. CH3COOH và HCOOCH3.
C. CH2 = CH – CH3 và CH2 = C(CH3)CH3.
D. CH3CH2CH2OH và CH3CH(OH)CH3.
II. PHẦN TỰ LUẬN. (3,0 điểm)
Câu 29. Buta-1,3-diene là một hydrocarbon được dùng nhiều nhất trong sản xuất cao su. Phân tử khối của của buta-1,3-diene gấp 1,6875 phân tử khối của oxygen.
Hãy lập công thức phân tử của buta-1,3-diene, biết kết quả phân tích nguyên tố của buta-1,3-diene có = 8.
Câu 30. Xác định loại đồng phân cấu tạo có thể có và viết các đồng phân cấu tạo có thể có của các hợp chất có công thức phân tử C4H10O.
Câu 31. Lưu huỳnh có nhiều ứng dụng trong đời sống và sản xuất. Người ta dùng lưu huỳnh để bảo quản thuốc bắc cũng như bảo quản hoa quả tươi lâu hơn. Hãy giải thích điều này. Việc làm này có gây hại gì cho sức khoẻ con người không?
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
Phần I: Trắc nghiệm
|
1 - A |
2 - D |
3 - D |
4 - B |
5 - C |
6 - B |
7 - A |
8 - A |
9 - A |
10 - B |
|
11 - A |
12 - A |
13 - D |
14 - A |
15 - A |
16 - B |
17 - B |
18 - D |
19 - C |
20 - A |
|
21 - C |
22 - C |
23 - D |
24 - C |
25 - D |
26 - B |
27 - B |
28 - B |
|
|
Phần II. Tự luận
Câu 29:
Dựa trên kết quả phân tích nguyên tố của buta-1,3-diene có = 8
nên %mc = 88,89% và %mH = 11,11%.
Buta-1,3-diene là một hydrocarbon nên có công thức phân tử là CxHy.
Vì phân tử khối của của buta-1,3-diene gấp 1,6875 phân tử khối của oxygen nên MButa-1,3-diene = 54. Ta có:
Công thức phân tử của buta-1,3-diene là C4H6.
Câu 30: C4H10O có các đồng phân về loại nhóm chức (alcohol và ether), mạch carbon và vị trí nhóm chức.
Các đồng phân:
Câu 31: Đốt cháy lưu huỳnh sinh ra khí SO2 độc. Tuy nhiên ở nồng độ thấp, khí này có tác dụng diệt khuẩn. Việc xông khí lưu huỳnh giúp việc bảo quản thuốc không bị mối mọt hay nấm mốc tấn công hoặc hoa quả tươi lâu hơn. Tuy nhiên, trong quá trình xông, lưu huỳnh sẽ lưu lại trên thuốc làm thuốc bị cứng, thay đổi màu sắc, mùi vị. SO2 gặp hơi ẩm trong phổi tạo thành H2SO3 ảnh hưởng đến phổi và hệ thần kinh, ...
S + O2 SO2
---HẾT---
................................
................................
................................
Trên đây tóm tắt một số nội dung miễn phí trong bộ Đề thi Hoá học 11 mới nhất, để mua tài liệu trả phí đầy đủ, Thầy/Cô vui lòng xem thử:
Tham khảo đề thi Hoá học 11 Chân trời sáng tạo có đáp án hay khác:
Để học tốt lớp 11 các môn học sách mới:
- Giải bài tập Lớp 11 Kết nối tri thức
- Giải bài tập Lớp 11 Chân trời sáng tạo
- Giải bài tập Lớp 11 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 11 (các môn học)
- Giáo án điện tử lớp 11 (các môn học)
- Giáo án Toán 11
- Giáo án Ngữ văn 11
- Giáo án Tiếng Anh 11
- Giáo án Vật Lí 11
- Giáo án Hóa học 11
- Giáo án Sinh học 11
- Giáo án Lịch Sử 11
- Giáo án Địa Lí 11
- Giáo án KTPL 11
- Giáo án HĐTN 11
- Giáo án Tin học 11
- Giáo án Công nghệ 11
- Giáo án GDQP 11
- Đề thi lớp 11 (các môn học)
- Đề thi Ngữ Văn 11 (có đáp án)
- Chuyên đề Tiếng Việt lớp 11
- Đề cương ôn tập Văn 11
- Đề thi Toán 11 (có đáp án)
- Đề thi Toán 11 cấu trúc mới
- Đề cương ôn tập Toán 11
- Đề thi Tiếng Anh 11 (có đáp án)
- Đề thi Tiếng Anh 11 mới (có đáp án)
- Đề thi Vật Lí 11 (có đáp án)
- Đề thi Hóa học 11 (có đáp án)
- Đề thi Sinh học 11 (có đáp án)
- Đề thi Lịch Sử 11
- Đề thi Địa Lí 11 (có đáp án)
- Đề thi KTPL 11
- Đề thi Tin học 11 (có đáp án)
- Đề thi Công nghệ 11
- Đề thi GDQP 11 (có đáp án)










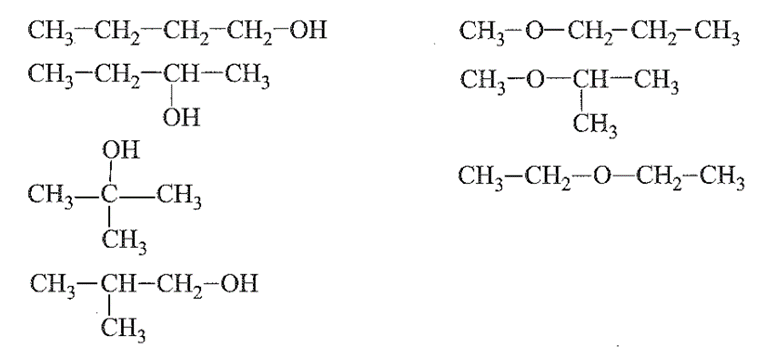





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

